티스토리 뷰
목차
유전자는 생명체의 정보를 저장하는 기본 단위로, 그 구조와 발현 조절은 생명 현상의 핵심 요소입니다. 본 글에서는 유전자의 기본 구조, 발현 조절 메커니즘, 후성유전학의 주요 개념과 인간 건강과 질병과의 관계를 심층적으로 살펴봅니다.
1. 유전자의 구조와 기본 구성
유전자는 생명체의 특성과 기능을 결정짓는 핵심 요소입니다. 유전자는 DNA의 특정 염기서열로 정의되며, 생체 기능을 위한 단백질 생성과 조절을 담당합니다. 인간 유전체는 약 20,000~25,000개의 유전자로 구성되며, 각각 고유한 역할을 수행합니다.
유전자는 크게 다음과 같은 구성 요소로 나뉩니다.
1) 엑손
엑손은 단백질로 번역되는 영역으로, 실제로 기능을 발휘하는 유전자의 핵심 부분입니다. 이 영역은 최종적으로 mRNA로 전사되어 단백질 합성에 관여합니다.
2) 인트론
인트론은 단백질로 번역되지 않는 영역이지만, RNA 스플라이싱 과정에서 중요한 역할을 합니다. 인트론은 유전자 발현 조절에도 기여합니다.
3) 조절 서열
프로모터, 인핸서, 억제자 등 조절 서열은 유전자 발현을 시작하거나 억제하는 데 중요한 역할을 합니다. 이러한 서열은 세포의 환경에 따라 유전자 발현을 동적으로 조절합니다.
유전자의 구조는 단순히 염기서열의 배열을 넘어, 다양한 조절 메커니즘과의 상호작용을 통해 생명체의 복잡성을 형성합니다.
2. 유전자 발현의 조절 메커니즘
유전자 발현은 특정 유전자가 언제, 어디서, 얼마나 활성화될지를 결정하는 복잡한 과정입니다. 세포는 다양한 조절 메커니즘을 통해 유전자 발현을 제어하며, 이를 통해 환경 변화에 적응하거나 생리적 균형을 유지합니다.
1) 전사 조절
유전자 발현의 가장 중요한 단계는 전사 조절입니다. 전사인자가 프로모터와 결합해 RNA 중합효소의 활성을 조절하며, 인핸서와 억제자 서열이 이 과정에 추가적인 영향을 미칩니다.
2) 후전사 조절
전사가 완료된 후에는 RNA 가공 단계에서 조절이 이루어집니다. 예를 들어, RNA 스플라이싱은 인트론을 제거하고 엑손을 연결해 다양한 단백질을 생성할 수 있도록 합니다.
3) 번역 조절
mRNA가 단백질로 번역되는 과정에서도 조절이 발생합니다. 특정 mRNA의 번역을 억제하거나 촉진하는 단백질 및 ncRNA가 관여합니다.
4) 후단백질 조절
단백질이 합성된 후에도 화학적 변형, 분해 조절 등이 단백질의 기능과 수명을 결정합니다.
유전자 발현 조절 메커니즘은 세포 수준에서의 정밀한 제어를 가능하게 하며, 생명체의 적응성과 복잡성을 증가시킵니다.
3. 후성유전학과 후성유전체의 개념
후성유전학은 유전정보 자체를 변경하지 않으면서 유전자 발현을 조절하는 메커니즘을 연구하는 학문입니다. 주요 후성유전학적 변화에는 DNA 메틸화, 히스톤 변형, 비암호화 RNA의 작용이 포함됩니다.
1) DNA 메틸화
DNA 메틸화는 특정 염기, 주로 시토신(C)에 메틸기가 부착되는 과정입니다. 이는 전사인자의 접근을 막아 유전자 발현을 억제하는 역할을 합니다. DNA 메틸화는 환경적 요인에 의해 변화할 수 있으며, 암이나 대사 질환과 같은 여러 질병과 연관되어 있습니다.
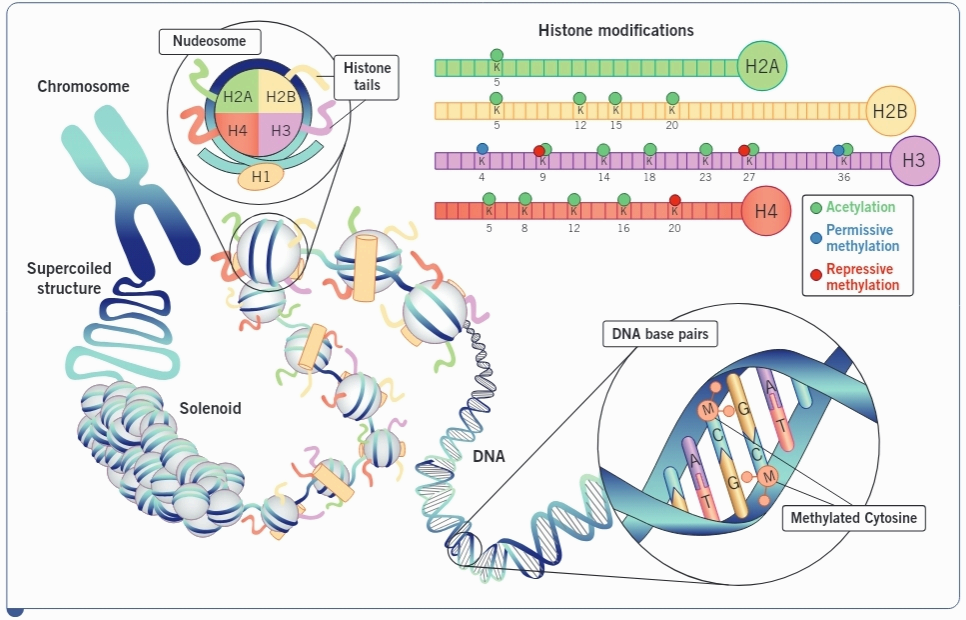
2) 히스톤 변형
히스톤 단백질의 화학적 변형(아세틸화, 메틸화 등)은 염색질 구조를 변화시켜 유전자의 접근성을 조절합니다. 예를 들어, 히스톤 아세틸화는 유전자의 활성화를 유도합니다.
3) 비암호화 RNA(ncRNA)
ncRNA는 유전자 발현을 직접적으로 조절하거나 RNA 안정성을 변화시킵니다. 마이크로 RNA(miRNA)는 특정 mRNA를 분해하거나 번역을 억제하는 방식으로 작용합니다.
4. 유전자의 구조적 조직화와 염색질의 3차원 구조
유전자는 뉴클레오좀이라는 기본 단위로 염색질에 조직화되어 있습니다. 뉴클레오좀은 DNA가 히스톤 단백질을 감싸는 구조로, 이는 염색질의 밀도와 유전자 발현을 조절합니다.
염색질은 진정염색질과 이질염색질로 나뉘며, 이들 간의 균형이 유전자 발현에 큰 영향을 미칩니다. 또한, 염색질의 3차원 구조는 유전자 간의 상호작용을 가능하게 하며, 세포가 특정 환경 자극에 반응할 수 있도록 돕습니다.
5. 후성유전학의 응용과 미래 전망
후성유전학 연구는 암, 신경계 질환, 대사 질환 등의 치료에 새로운 가능성을 열고 있습니다.
예를 들어, DNA 메틸화 패턴 분석은 특정 암의 초기 진단에 활용될 수 있으며, 히스톤 변형 조절제는 항암제로 개발되고 있습니다. 또한, 비암호화 RNA를 활용한 맞춤형 치료법은 유전적 변이와 질병 간의 관계를 더 잘 이해하고 해결하는 데 도움을 줍니다.
후성유전체 연구는 유전학의 패러다임을 바꾸고 있으며, 인간 질병의 이해와 치료를 위한 새로운 길이 될 것입니다.
결론
유전자의 구조와 발현 조절, 그리고 후성유전학적 메커니즘은 생명체의 복잡성을 이해하는 열쇠입니다. 이러한 연구는 의학과 생명과학의 발전에 큰 기여를 하고 있으며, 개인 맞춤형 치료와 신약 개발의 새로운 장을 열고 있습니다.
'health > genetic counseling' 카테고리의 다른 글
| 인간 유전체 (기능, 미토콘드리아 DNA, 비부호화 서열) (0) | 2025.01.21 |
|---|---|
| 염색체란? (정의, 구조, 유형) (0) | 2025.01.21 |
| 핵산과 유전자 발현 (구조, DNA복제, RNA전사) (0) | 2025.01.20 |
| 유전 상담의 국제적 현황 (미국, 유럽, 아시아의 사례) (0) | 2025.01.18 |
| 유전 상담의 새로운 패러다임 (의료 시스템, 통합, 전망) (0) | 2025.01.18 |
